台灣每年約有600名新的惡性腦瘤病人,其發生率雖不在10大癌症之內,然而死亡率卻不低,確診後存活期間極短,僅約一年至兩年的餘命。長庚醫院攜手成大醫工跨領域合作,成功開發創新的類病毒奈米載體,可攜帶治療用核酸片段,抑制腫瘤特定基因表現,增強放射治療效果,動物實驗顯示能延長腦瘤小鼠兩倍的存活期,治療效果顯著。研究成果已發表在2023年6月美國化學學會《ACS Nano》頂尖期刊,創新概念更獲選為期刊封面故事,並榮獲2023年國家新創獎肯定,未來極具高度臨床應用潛力,有望克服現腦瘤治療的困境。
惡性腦瘤其致病機轉至今未明,難以預防且治療困難。惡性腦瘤常見的症狀包括頭痛、噁心、嘔吐。腫瘤壓迫周邊正常組織可引起抽搐或癲癇、肢體無力、偏癱、視力模糊和感覺障礙等症狀。腫瘤侵犯小腦則會損害運動功能或平衡感,造成步態不穩或運動失調。患者的心智狀態也可能出現變化,表現為失語、記憶力下降、注意力不集中、情緒或人格改變等症狀。患者罹病後發生殘障、失能的機率極高,是國人健康的重大威脅。
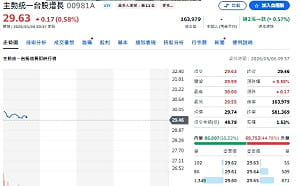
全站首選:瑤姐再出手!00981A「增1、加39、減2」全鏈掃貨 聯電成大亮點
惡性腦瘤治療困難的主要原因是因其具有迅速增生惡化的特性,腫瘤結構複雜有如八爪章魚般的浸潤生長在正常的腦組織之間,而且沒有明確清楚的界限區分,導致手術難以完全清除造成大多數的惡性腦瘤預後很差,即使術後經積極的放射線治療、化學治療後仍會復發。由新北市立土城醫院副院長、也是林口長庚醫院神經外科魏國珍教授領導的研究團隊,與成功大學醫工系楊閎蔚教授攜手合作,長期致力開發新穎材料及藥物載體以治療惡性腦瘤。
魏國珍教授表示,目前對腦瘤的治療始終效果不好,病人存活期平均只有約14到16個月,主要原因是腦瘤細胞具有詭譎多變的異質特性,其強大基因自我修復能力造成放射治療及藥物治療的效果不佳。因此,團隊以人工智慧開發類病毒奈米載體來有效傳遞治療用干擾核酸,以抑制腫瘤細胞基因表現,大幅提升惡性腦瘤的治療效率。這種藉基因表現調控機制抑制某一基因表現的現象,就是所謂的基因靜默。
魏國珍教授指出,長庚醫院與成功大學研究團隊利用腦瘤小鼠做為測試模型,利用增強對流傳輸法,直接將類病毒藥物載體精準注射傳遞到腦瘤區域;結果顯示腦瘤細胞中負責DNA修復的基因表現成功被抑制,阻斷腦瘤細胞自我修復能力,使腫瘤顯著縮小。而將此基因載體與低劑量放射治療同步施用,可以使腦瘤小鼠的存活期增加兩倍,不但提升了放射線治療效果,同時也降低放射治療劑量以減少其副作用。在動物實驗極具潛力的研究成果,揭露其未來臨床應用的高度可能性。
現正最夯:中國精心策畫「鎖死台灣」矢板明夫:習近平霸王硬上弓鬧國際笑話
更特別的是,研究團隊應用特殊模組化的治療用核酸骨架設計,針對不同種類的疾病,或是病人特殊的基因選擇接上應對的干擾核酸,可完美應用於個人化精準醫療。此特殊設計的基因工程技術,更可大幅簡化類病毒載體的合成過程,提升製作效率及降低成本。
而這項研究成果榮獲美國國家化學學會官方期刊,也是奈米、奈米製造技術與奈米科學領域頂尖期刊《ACS Nano》的重視,被選為封面故事。魏國珍教授表示,研究工作橫跨四年時間,從開發模組、基因載體合成測試、體外細胞試驗、動物實驗驗證等,團隊成員緊密結合,由臨床角度審視需求,自醫工層面提出材料設計解決方案,並完整驗證其效應,為目前跨領域合作的優良典範。
長庚醫院與成功大學團隊研究成果同時也獲國科會化學圖書服務計畫電子報報導,以宣傳台灣醫學與工程跨領域合作之創新發現,並榮獲2023年國家新創獎,充份展現其未來應用於產業的高度價值。目前已獲醫藥產業洽談合作技轉事宜,未來將有機會改善目前腦瘤治療的困境。

這項研究成果榮獲美國國家化學學會官方期刊《ACS Nano》的重視,被選為封面故事。 圖:長庚醫院/提供