國產疫苗緊急授權EUA審查即將展開,近日卻被爆負責審查的「疫苗療效評估專家會議」中有半數委員遭到替換。對此,立委高虹安於今日在臉書發文,以「考卷作答一半就想交,還可以自己換閱卷委員?這樣的答卷內容品質有多高、批改出來的分數又是否可信?」比喻政府的舉措,並希望食藥署能盡快出面回應,公布審查委員名單。
高虹安在臉書上進一步提出國產疫苗的5大疑慮:
一、採購決策過程急於一時,採購當下法源依據、預算來源支吾其詞,始終沒有明確答案。
二、陳時中部長立院答詢脫口而出:國際疫苗超過空窗期「我們也不要了」,被質疑是為國產疫苗背書。
三、食藥署匆忙於6月10日高端疫苗解盲當天早上提出EUA標準,選用全球民主法治國家皆尚未採用的指標,亦即以「免疫橋接」取代三期臨床試驗,除了疑似改抄寫美國FDA部分EUA標準內容,更少了美國FDA規定所需要的「保護力達50%的效力保證 (Efficacy)」。
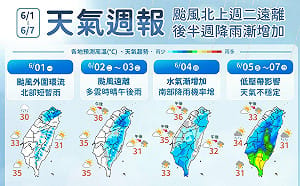
當前熱搜:下週天氣轉不穩!週四起水氣增 週末防雷雨及局部大雨
四、高端疫苗解盲只證明安全性,高端疫苗以武漢病毒株為基底的「中和抗體效價」做指標僅能參考,無法證明疫苗具有保護力。
五、高端疫苗趕在6月15日遞交EUA申請書,但是否能在七月如期施打?重點是能否走完EUA程序。而蔡總統原本說過七月開打國產,近日則又改口「沒有說一定要什麼時候」。
高虹安說她回想起,上周在立院特別預算的協商中,在野黨提出的國產疫苗EUA審查資訊公開遭到否決,連要求公開會議紀錄都被加上必須「審查結束後兩週內、去識別化」才能公開的不合理條件。這些迴避公開透明的舉措為國人對疫苗公信力產生質疑的主因。除此之外,她更進一步舉出德國mRNA疫苗採簡易審查而導致不良後果的案例,希望政府能以此為借鏡。
最後她提出,若媒體報導的評委大換血的消息為真,即便國產疫苗通過EUA審查,公信力也蕩然無存,並且呼籲政府趕快出面回應國產疫苗的相關質疑,以公開透明的方式審理。切勿以政治取代科學,才是對國人生命健康的負責任作為。

高虹安於今日在臉書發文,提出對國產疫苗審查的疑慮。 圖: 翻攝自高虹安臉書

高虹安於今日在臉書發文,提出對國產疫苗審查的疑慮。 圖: 翻攝自高虹安臉書