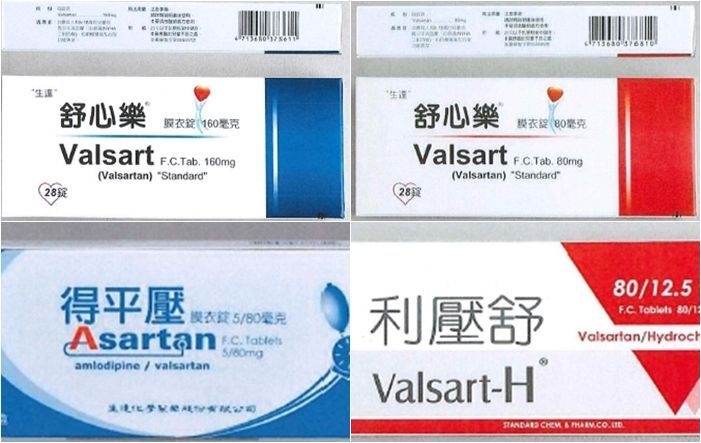
中國近日來發生的疫苗安全問題,突顯中國藥品監管體系不力風險,同時,中國作為全球最大的原料藥供應國,國際客戶開始對中國藥品品質產生疑慮。
原料藥又稱活性藥物成份,需經過加工,才製成可直接使用的藥物。英國金融時報中文網報導,根據英國藥品監管機構的數據,中國製造商佔全球原料藥產量的40%。
當前熱搜:台股開盤》43000保衛戰開打!有待台積點火 分析師:這時間前難脫震盪
7月,歐洲藥品管理局(EMA)與美國食品藥品管理局(FDA)針對一種由中國浙江華海藥業生產、用於生產降壓藥的原料含有致癌雜質發出警告,導致一系列受影響藥物被召回。
隨後,北京方面宣布,中國售出了數十萬支不合格的疫苗,引起了公眾的強烈抗議。製藥公司長生生物科技的高階主管被逮捕,該公司也被當局指控在狂犬疫苗生產過程中偽造數據。
報導說,中國擁有數千家原料藥生產商,去年的原料藥出口額達290億美元,中國的生產商還為梯瓦製藥(Teva Pharmaceutical)等學名藥製造商以及強生(Johnson & Johnson)、諾華(Novartis)等跨國公司供應原料。據業內估計,在美國使用的原料藥中,約有80%來自中國和印度。
現正最夯:川普下令再度攻擊伊朗!美股道瓊暴跌953點、台積電ADR跌4.48%
但報導引述安永駐中國的合夥人林江翰表示,「許多(中國)原料藥公司沒有嚴格遵循既定的(製造)流程,也不嚴格記錄數據。」、「由於人手不足,監管當局沒有對原料藥生產商進行足夠的抽查。」
報導說,FDA對中國製藥企業發出的警告數量從2014年的5次躍升至去年的22次,收到警告是被放入進口黑名單的前奏。印度企業也經常收到警告,但過去2年,中國企業收到的警告比印度企業多。
根據EMA的數據,歐盟國家的監管機構每年對中國原料藥生產商進行20至40次檢查,其中約10%的檢查中發現不合規的情況。
但報導表示,中國正在努力改善現狀。2015年,中國國家食品藥品監督管理總局推出新的監管框架並得到認可:中國成為全球藥品標準機構「國際醫藥法規協和會」(ICH)的第8個成員國。
耶魯大學公共衛生學院教授陳希說,近期的疫苗醜聞「可能是中國製藥行業的一個重大挫折」;但另一方面,這次危機也可能是中國政府改革的契機。