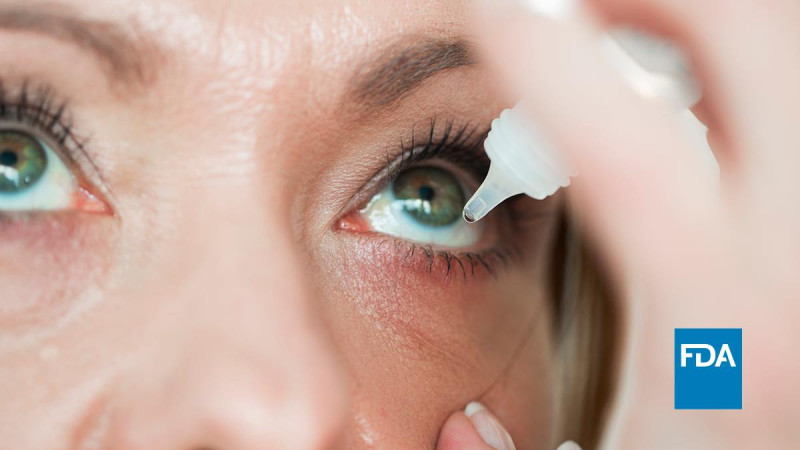
印度藥廠曾因出現「感染、失明」等因素而回收人工淚液,美國食品暨藥物管理局(FDA) 22 日再度針對同廠牌的「眼膏」啟動召回程序,原因稱可能有細菌感染疑慮,這已是該廠商第三款被召回產品。
據美媒報導,美 FDA 發布消息稱,「建議」環球製藥保健公司(Global Pharma Healthcare)召回 Delsam Pharma 眼膏Artificial Eye Ointment ,該公司同意並啟動了召回。
來自印度的環球製藥與之前被要求召回的 EzriCare 、 Delsam Pharma 人工淚液來自同一製造商。
美 FDA 這次表示,產品中可能存在細菌污染,並未提供更多細節。
美 FDA 在先前聲明中曾表示,使用受污染的人工淚液,會增加眼睛感染的風險,甚至可能導致失明或死亡。有眼睛感染跡象或相關症狀的患者,應與他們的醫療保健提供者就此進行討論,或立即尋求醫療幫助。
全站首選:大雨狂炸!全台狂灌2.5億噸水 「4水庫」蓄水率衝破90%
截至 2 月 21 統計數據中,美國疾病管制暨預防中心(CDC)表示,大約已確認有 58 名病人與這次病菌感染的爆發有關,至少有 16 名患者因感染而住院,感染者分布在國內十幾個州。
目前也因環球製藥多次違規與缺乏適當的微生物測試等規範,被禁止再向美國進口藥物。
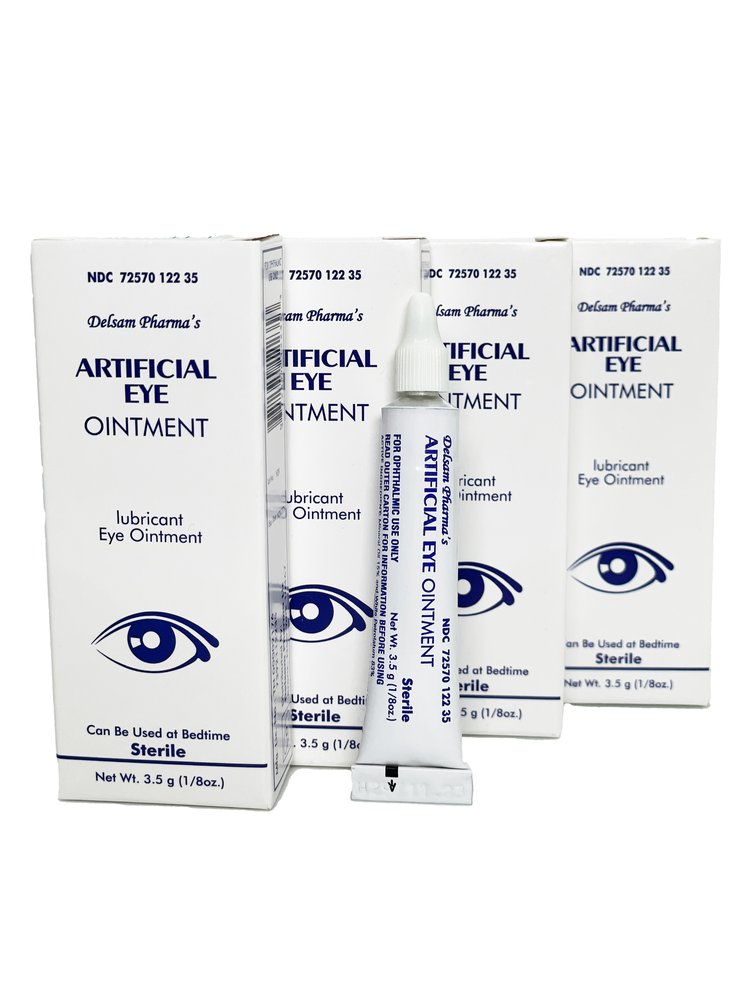
環球製藥所製造的「Artificial Eye Ointment」眼膏被美FDA認為有細菌感染疑慮。 圖:翻攝自Delsam Pharma 官網(資料照)
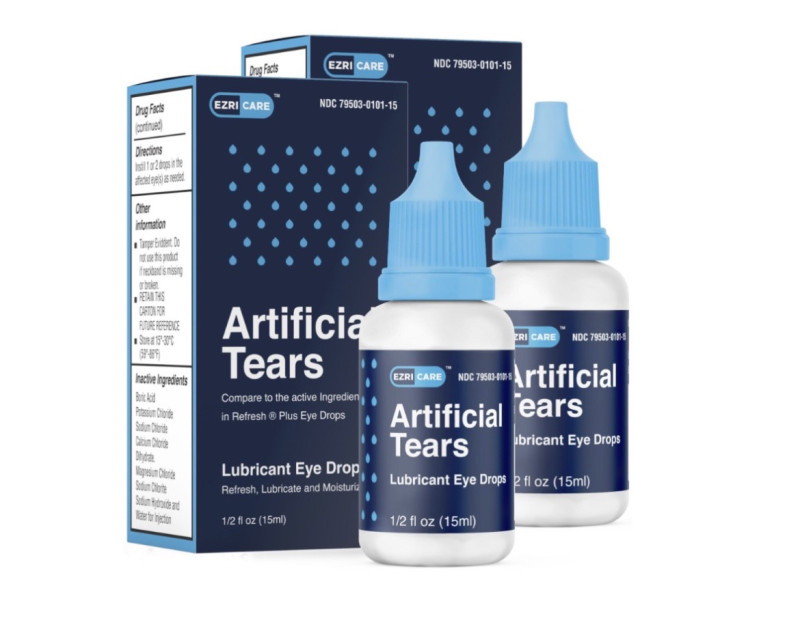
「EzriCare」推出的人工淚液,被調查出瓶子中含群聚感染的病原體「綠膿桿菌」。 圖:翻攝自EzriCare官網(資料照)